Obsah
- stupňa
- Metóda 1 Naučte sa pravidlá rozpustnosti
- Metóda 2 Použite mnemotechniku: NAG SAG
- Metóda 3 Základy učenia
Rozpustnosť zlúčeniny je jej schopnosť sa rozpúšťať vo vode. Nerozpustná zlúčenina bude tvoriť zrazeninu v roztoku. Uvádza sa tiež, že čiastočne rozpustná zlúčenina je chemicky nerozpustná. Ak si pamätáte pravidlá rozpustnosti, uľahčí vám to život, keď musíte pracovať s chemickými rovnicami. S trochou času, práce a niektorých mnemotechnických trikov si budete pamätať všetky vzorce.
stupňa
Metóda 1 Naučte sa pravidlá rozpustnosti
-

Soli skupiny 1A sú rozpustné. Periodická tabuľka prvkov je usporiadaná do riadkov a stĺpcov nazývaných „obdobia“ a „skupiny“. Prvý stĺpec tabuľky obsahuje prvky skupiny 1A. Sú to alkalické kovy. Patria sem prvky Li, Na, K, Cs a Rb.- Príklad: KCl a LiOH sú rozpustné vo vode.
-

Soli dusičnanov, chlorečnanov a acetátov sú rozpustné. Keď dusičnany (vzorca NO3), chlorečnan (vzorec C103) alebo laketát (vzorca CH3COO) tvoria soli, stávajú sa rozpustnými vo vode.- Príklad: KNO3, NaClO3 a CH3COONa sú všetky rozpustné.
-

Všetky amónne soli sú rozpustné. Amónny lev (vzorec NH4) tvorí soli, ktoré sa úplne disociujú vo vode. Neexistuje žiadna výnimka z tohto pravidla.- Príklad: NH4OH je rozpustný, aj keď obsahuje hydroxidový ión.
-
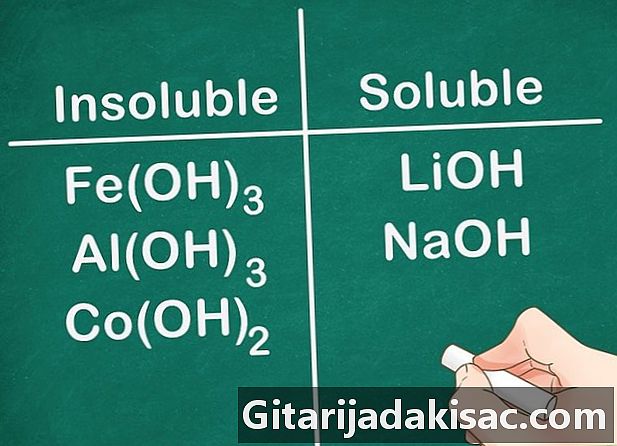
Väčšina hydroxylových zlúčenín je nerozpustná. Niektoré hydroxidové soli sú mierne rozpustné. Toto je prípad hydroxidov vytvorených s prvkami skupiny 2 (Ca, Sr a Ba). Hydroxidové soli tvorené prvkami skupiny 1 sú výnimkou, pretože tieto prvky sú stále rozpustné.- Príklad: Fe (OH)3, Al (OH)3 a Co (OH)2 sú nerozpustné, ale LiOH a NaOH sú rozpustné.
-

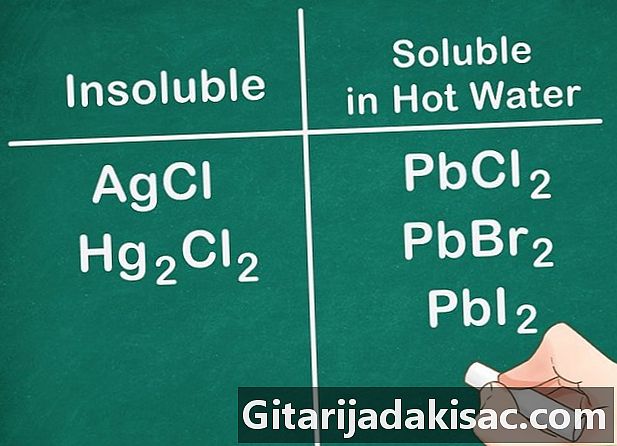
Nekovové soli skupiny 17 sú všeobecne rozpustné. Nekovy skupiny 17 zahŕňajú chlór (Cl), bromid (Br) a liódu (I). Výnimky z tohto pravidla sú peniaze, olovo a ortuť. Zlúčeniny pozostávajúce z týchto nekovov a týchto iónov nie sú rozpustné.- Príklad: AgCl a Hg2cl2 sú nerozpustné.
- PbCl2, PbBr2 a Pbl2 sú rozpustné vo veľmi vysokej vode.
-
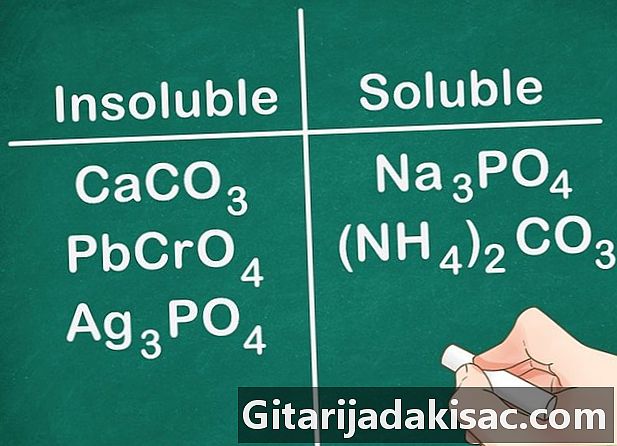
Väčšina uhličitanov, chromátov a fosfátov je nerozpustná. Chemické vzorce pre tieto prvky sú: CO3 (uhličitany), CrO4 (chromáty) a PO4 (Fosfáty). Kovy skupiny 1A a zlúčeniny NH4 výnimka a sú rozpustné.- Príklad: zlúčeniny ako CaCO3, PbCrO4 a Ag3PO4 sú všetky nerozpustné, zatiaľ čo zlúčeniny ako Na3PO4 a (NH4)2CO3 sú rozpustné.
-
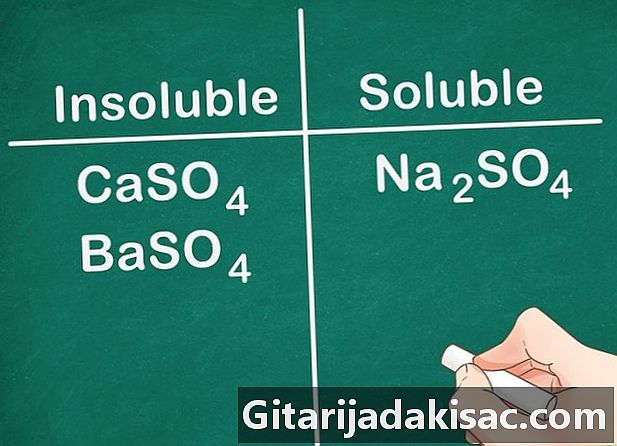
Väčšina síranových solí je rozpustných. Väčšina solí vrátane SO iónu4 je rozpustný vo vode. Výnimky z tohto pravidla sú Ca, Ba, Pb, Ag, Sr a Hg. Sulfátové soli obsahujúce tieto ióny nie sú rozpustné.- Príklad: Na2SO4 je úplne rozpustný, zatiaľ čo CaSO4 a BaSO4 nie sú rozpustné.
-

Väčšina zlúčenín síry je nerozpustná vo vode. Výnimkou z tohto pravidla sú bárium, vápnik, horčík, sodík, draslík a amoniak. Vo vode sú rozpustné iba zlúčeniny vyrobené z týchto prvkov a sulfid.- Príklad: CdS, FeS a ZnS sú všetky nerozpustné.
- Sulfidy prechodných kovov sú však nerozpustné.
Metóda 2 Použite mnemotechniku: NAG SAG
-

Použite mnemotechniku NAG SAG mnemotechniku. Lacronyme NAG SAG je ľahký trik na zapamätanie rozpustných zlúčenín a výnimiek. Napíšte meno NAG SAG a zapamätajte si význam každého písmena. Táto technika nevylučuje všetky pravidlá týkajúce sa rozpustnosti, ale pokrýva ich dobrú časť. Všetky písmená predstavujú rozpustné molekuly.- N: Dusičnany (NO3)
- A: Acetáty (CH3COO)
- G: Alkalické kovy skupiny 1 (Li, Na, atď.)
- S: Sírany (SO4)
- A: Amónne ióny (NH4)
- G: nekovy skupiny 17 (F, Cl, Br, I atď.)
-

Nezabudnite na názov PMA pre prvú výnimku. P predstavuje Pb (olovo). M predstavuje ortuť (Hg2). A predstavuje striebro (Ag). Tieto tri ióny nie sú nikdy rozpustné v sulfátovej skupine alebo s kovmi zo skupiny 17.- Ak si všimnete mnemotechnický trik, nakreslite hviezdu blízko skratky PMA a podobnú hviezdu blízko S a G SAG, aby ste si pripomenuli, že ide o výnimky.
-

Nezabudnite na slová „Castro“ a „bar“ pre druhú výnimku. Môže to znieť hlúpo, ale tieto slová vám pomôžu zapamätať ióny vápnika (Ca, stroncium (Sr) a bárium (Ba).). Tieto tri ióny nie sú nikdy síranmi rozpustné.- Urobte krížik vedľa týchto slov a ďalší krížik blízko SAG, aby ste si uvedomili, že tieto ióny sú výnimkou pre rozpustnosť síranu.
Metóda 3 Základy učenia
-

Preskúmajte často. Zapamätanie si informácií vždy vyžaduje čas a prácu. Čím viac hodín čítate, tým viac si budete pamätať z dlhodobého hľadiska. Pravidelne si prečítajte pravidlá a každý deň si vyskúšajte danú tému.- Požiadajte priateľov alebo rodinu, aby sa vás na túto tému opýtali pri obede alebo večeri.
- Keď budete mať voľný čas, uschovajte si kópiu pravidiel na kontrolu.
-

Vytvorte súhrnné listy a použite ich. Karty sú vynikajúcim médiom na rýchle prehodnotenie a zapamätanie si predmetu. Všimnite si pravidlá rozpustnosti na kartách s niekoľkými príkladmi. Prezrite si hárky, kým nebudete oboznámení s pravidlami a názvami zlúčenín, ktoré sú rozpustné a nerozpustné.- Vezmite si karty so sebou a vyberte ich na kontrolu v aute alebo počas čakania na svojich priateľov.
- Všetky príležitosti sú vhodné na kontrolu vašich záznamov.
-

Použite mnemotechnické prostriedky. Mnemotechnické nástroje sú tipy, ktoré vám pomôžu rýchlo a ľahko zapamätať informácie. Keď sa naučíte mnemotechnický výraz, môže byť užitočné napísať ho niekoľkokrát, aby ste si ho pamätali. Mnemotechnické triky sú užitočné iba vtedy, ak viete, čo znamená každé písmeno!- Precvičujte si písanie skratiek a čo znamená každé písmeno.
- Keď práve prebieha kontrola, najprv si všímajte mnemotechnické tipy pre budúce použitie.